El logro publicado en línea el 29 de enero en Informes celulares, elimina un obstáculo importante para los científicos que buscan identificar las causas del Alzheimer esporádico y encontrar medicamentos que puedan prevenir o revertir sus devastadores efectos neurodegenerativos.
El trabajo también proporciona información sobre los primeros cambios moleculares que pueden conducir al Alzheimer y apunta a un posible objetivo terapéutico.
Se estima que la enfermedad de Alzheimer afecta a 5.7 millones de personas en los Estados Unidos. Hasta ahora, la mayoría de los modelos de “Alzheimer en una placa de Petri” se han derivado del Alzheimer familiar, una forma rara de la enfermedad que se transmite de padres a hijos, está causada por mutaciones genéticas dominantes y a menudo se manifiesta antes de los 65 años.
Por el contrario, se cree que la forma esporádica surge de una serie de factores de riesgo genéticos y ambientales que aún no se comprenden del todo.
El nuevo modelo “es un intrigante sistema in vitro que faltaba en este campo”, afirmó el autor principal del estudio. Bruce Yankner, profesor de genética en el Instituto Blavatnik de la Facultad de Medicina de Harvard, quien, en la década de 1990, dirigió el equipo que demostró por primera vez los efectos tóxicos de la beta amiloide, el sello distintivo del Alzheimer.
Utilizando su nuevo modelo, Yankner y sus colegas identificaron cambios en las células madre neurales durante las primeras etapas del desarrollo —entre ellos, una diferenciación acelerada y anomalías en una proteína que se cree que protege contra el deterioro cognitivo relacionado con la edad— que pueden aumentar la probabilidad de desarrollar Alzheimer más adelante en la vida.
“Es emocionante descubrir un fenotipo compartido”, afirmó Yankner. “Fue algo inesperado”.”
Divergencia dramática
Yankner y sus colegas comenzaron por obtener células cutáneas de cinco personas con Alzheimer esporádico y seis personas sanas de la misma edad. Revertieron estas células adultas a un estado anterior, indiferenciado. Estas células madre pluripotentes inducidas (iPS) pueden dar lugar a muchos otros tipos de células.
Al principio, las células derivadas del Alzheimer y los controles parecían indistinguibles. Pero cuando el equipo las indujo a madurar hasta convertirse en progenitores neurales —células madre que dan lugar a la mayoría de los tipos de células del cerebro—, surgieron diferencias dramáticas.
Los análisis de ADN revelaron que las células del Alzheimer presentaban una actividad inusualmente alta en genes relacionados con la diferenciación neuronal, la creación de neuronas y la formación de conexiones entre neuronas.
Esos resultados sugerían que las células progenitoras del Alzheimer se convertirían en neuronas maduras mucho antes que sus homólogas sanas y, de hecho, eso es lo que observaron los investigadores en las placas de laboratorio.
“Las células se diferencian ‘mejor’, o al menos más rápido”, afirmó Yankner. “Se obtienen más neuronas, no menos”.”
Las células derivadas del Alzheimer también se volvieron eléctricamente excitables, o capaces de comunicarse entre sí, antes y con más vigor que las células de control.
Planteando preguntas a REST
Yankner buscó respuestas en una proteína llamada REST. La proteína tenía un interés especial por dos razones: porque se sabe que regula la diferenciación neural durante el desarrollo temprano y porque Yankner había demostrado anteriormente que, tras desaparecer en la primera infancia, la REST reaparece en el cerebro envejecido con el potencial de proteger contra la neurodegeneración y otras tensiones.
Efectivamente, las células de Alzheimer que se diferenciaban prematuramente tenían menos REST en sus núcleos que las células normales. El REST que quedaba no se unía a los genes y no funcionaba con normalidad.
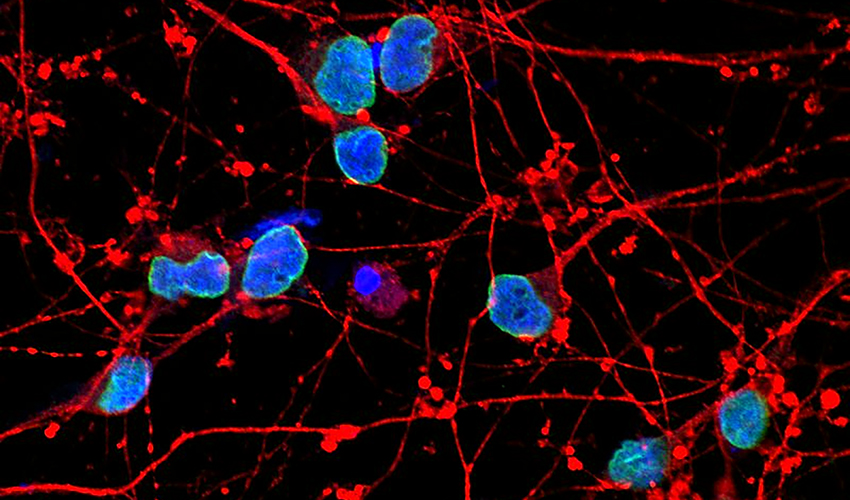
Los investigadores también descubrieron que los núcleos de las células con Alzheimer presentaban con mayor frecuencia deformaciones y cambios estructurales en sus membranas que las células normales. Investigaciones anteriores habían detectado estos defectos en los cerebros de personas fallecidas con Alzheimer, pero aún no se sabía con certeza cómo se relacionaban con la neurodegeneración ni si realmente lo hacían.
Los investigadores se preguntaron si la constelación de anomalías —desde la actividad genética hasta la diferenciación prematura, pasando por los bajos niveles de REST y los defectos del núcleo celular— podría estar provocada por la beta amiloide tóxica, la proteína conocida por su implicación en el desarrollo del Alzheimer. Sin embargo, cuando los investigadores detuvieron la producción de la proteína amiloide, no se produjo ningún cambio.
¿Qué hay de la proteína tau fosforilada, la base de los llamados ovillos neurofibrilares que se encuentran en el cerebro de los pacientes con Alzheimer? La respuesta, una vez más, fue no: los cambios se produjeron antes de que apareciera cualquier proteína tau anómala en las células.
Revisión de la realidad
Las diferencias entre las células esporádicas de Alzheimer y las células normales eran tan notables que los investigadores se preguntaron si habían cometido un error al reprogramar las células madre.
“Al principio, era escéptico respecto a que pudiera existir un defecto tan profundo en el Alzheimer esporádico, en el que no hay una mutación genética dominante”, afirmó Yankner.
Sin embargo, al asociarse con colegas de varias instituciones, los investigadores pudieron replicar sus hallazgos en células iPS normales y esporádicas de Alzheimer obtenidas de otros tres laboratorios; en células madre editadas para tener el APOE4variante genética, el factor de riesgo genético más común para el Alzheimer; y en organoides cerebrales, pequeñas estructuras similares al cerebro creadas a partir de células iPS cultivadas en andamios tridimensionales.
Los estudios de perfil genómico sugirieron que REST era el regulador genético con mayor probabilidad de verse alterado en los organoides con el APOE4 mutación, seguida de otras dos proteínas que interactúan con REST.
Los organoides son una tecnología muy interesante para investigar los primeros eventos del desarrollo neurológico, afirmó Yankner.
Coautor del estudio George Church, profesor Robert Winthrop de Genética en el Instituto Blavatnik de la Facultad de Medicina de Harvard, está entusiasmado con el potencial de esta tecnología para descubrir más rápidamente los factores que contribuyen a enfermedades que no tienen causas genéticas claras y que tardan más de medio siglo en manifestarse en los seres humanos.
“No solo podemos crear tipos de células humanas adecuadas, sino que incluso podemos saltarnos las muchas décadas que normalmente se necesitan para desarrollar un fenotipo y encontrar ensayos que detecten la predisposición a enfermedades de aparición tardía, incluso cuando la genética conocida es insuficiente”, afirmó.
Juventud y edad
El estudio plantea dos puntos contrarios a la intuición: en primer lugar, que los orígenes de una enfermedad que afecta a los adultos mayores pueden tener su origen en el desarrollo temprano y, en segundo lugar, que las células cerebrales derivadas de pacientes con neurodegeneración se desarrollan más rápido, y no más lento, que las células normales.
Yankner se pregunta si la rápida maduración de las neuronas en los pacientes con Alzheimer hace que su reserva de células madre neuronales se agote en la edad adulta antes que en las personas que no padecen neurodegeneración. Otra posibilidad es que la diferenciación acelerada de las células madre neuronales perjudique la recuperación de la memoria en los adultos al alterar los circuitos neuronales establecidos, afirmó.
Es igualmente posible, dijo Yankner, que los fenómenos observados por su equipo no causen directamente el Alzheimer, sino que lo anuncien. Si es así, estos cambios podrían servir como marcadores tempranos de la enfermedad, como una oportunidad para intervenir antes de que aparezcan los síntomas y como una forma más fácil y rápida de buscar nuevos tratamientos.
Otros estudios abordarán estas y otras cuestiones.
Aunque el nuevo modelo representa un gran avance para la investigación sobre el Alzheimer, es poco probable que sea el capítulo final de la historia.
“Estos modelos de cultivo de células iPS son valiosos porque se derivan de células humanas y reproducen el desarrollo. Sin embargo, no han envejecido 80 años como un cerebro con Alzheimer”, afirmó Yankner.
Sin embargo, añadió, este nuevo recurso ya ha comenzado a impulsar una serie de nuevas investigaciones que, según espera, profundizarán nuestra comprensión de una enfermedad compleja y, en última instancia, mejorarán la vida de las personas.
Financiación y autoría
Katharina Meyer, becaria posdoctoral del laboratorio Yankner, y Heather Feldman, antigua estudiante de posgrado del laboratorio Yankner que ahora trabaja en el Centro de Investigación Oncológica Fred Hutchinson de Seattle, son las coautoras principales del artículo. Otros autores están afiliados a la Facultad de Medicina de Harvard, el Instituto Wyss de Ingeniería de Inspiración Biológica, la Universidad Putra de Malasia y el Instituto Picower para el Aprendizaje y la Memoria del MIT.
Este trabajo ha sido financiado por los Institutos Nacionales de Salud (subvenciones DP1OD006849, R01AG046174, RF1AG048056, R01AG046174, RF1AG048029 y RM1HG008525), la Fundación Paul F. Glenn para la Investigación Médica, la Iniciativa de Investigación Fidelity Biosciences, la Fundación Robert A. y Renee E. Belfer Family y el Fondo Cure Alzheimer.
Fuente: https://hms.harvard.edu/news/sporadic-alzheimers-dish


